近日,四川农业大学动物医学院动物医学免疫学系陈舜/程安春团队在国际微生物学权威期刊mBio上发表了题为“TRIM25 promotes antiviral innate immune response by stabilizing IRF7 and its nuclear translocation”(TRIM25调控IRF7稳定及其核转位促进抗病毒先天免疫反应)的研究论文。该研究揭示了TRIM25在禽类抗病毒信号通路中的核心激活作用,为理解禽类的抗RNA病毒免疫提供了全新的分子解释。
天然免疫是宿主抵抗病原微生物入侵的第一道防线。在哺乳动物中,IRF3是启动早期抗病毒干扰素反应的关键转录因子。然而,大多数禽类在进化过程中缺失了IRF3基因,IRF7因此承担了更为核心和广泛的抗病毒免疫调控功能。尽管如此,禽类IRF7是如何被精确调控以应对病毒威胁的,其分子机制尚不完全明确。
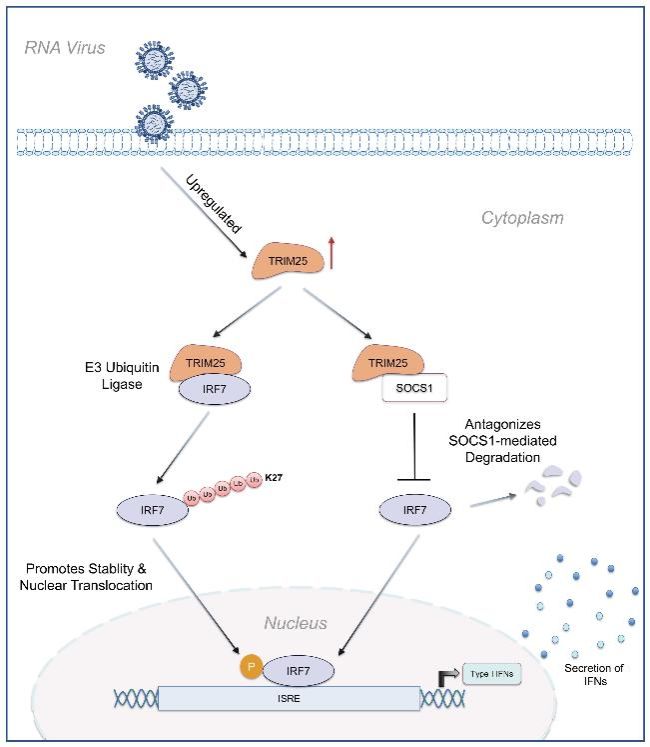
本研究深入探究了鸭TRIM25在调控IRF7及抗RNA病毒天然免疫中的关键作用。研究发现,TRIM25发挥E3泛素连接酶活性,通过催化IRF7第46位赖氨酸发生K27泛素化修饰,从而促进IRF7的稳定性及其向细胞核的转位。此外,TRIM25还能以不依赖其E3连接酶活性的方式,通过拮抗SOCS1介导的降解途径来进一步稳定IRF7蛋白。这两种机制共同促进了I型干扰素的高效表达,并在鸭胚成纤维细胞及雏鸭体内显著限制了多种RNA病毒的复制。该研究系统解析了禽类TRIM25双重靶向调控IRF7的独特机制,揭示了禽类在缺失IRF3的进化背景下,利用TRIM25-IRF7轴实现高效抗病毒防御的代偿性免疫策略。
四川农业大学动物医学院吴震副教授与硕士研究生崔颖瑄为该论文的共同第一作者,陈舜教授与程安春教授为共同通讯作者。该研究得到了国家自然科学基金(32302885,32272976,32470142,32302848)、国家现代农业产业技术体系(CARS-42-17)、四川省兽药创新团队(SCCXTD-2021-18)及四川水禽产业创新团队(SCCXTD-2024-25)项目的资助。
原文链接:https://doi.org/10.1128/mbio.00470-26

