(学校新闻报道:https://news.sicau.edu.cn/info/1078/85237.htm)
11月28日,我院预防兽医系动物寄生虫病研究中心李威教授与欧洲分子生物学成像中心(EMBL Imaging Center)Simone Mattei博士、德国慕尼黑大学实验寄生虫中心(LMU Experimental Parasitology)Elena Jimenez-Ruiz博士、Markus Meissner教授合作,在国际权威期刊《Nature Communications》上发表了题为“An apical ring protein essential for conoid complex assembly and daughter cell formation in Toxoplasma gondii”(极环蛋白调控弓形虫类锥复合体组装及子代细胞形成)的研究论文。该研究揭示了CGP和ASAF1两个关键蛋白在弓形虫新生类锥复合体组装过程中的重要作用,为开发新型抗弓形虫药物提供了重要潜在靶点。李威教授为本论文的第一作者兼并列通讯作者。
弓形虫作为顶复门原虫的模式生物,其顶端的类锥复合体(conoid complex)是介导弓形虫滑行运动、入侵宿主细胞及逸出的核心结构,由极环(APR)、前类锥体环(PCRs)、类锥体(conoid)等组成。然而,该结构组装的分子机制尚不完全明确。
本研究以速殖子为研究对象,利用CRISPR/Cas9基因编辑、超高分辨显微成像、冷冻电子断层扫描(cryo-ET)及邻近标记法(BioID)等前沿技术,发现:1)ASAF1是首次鉴定的子代虫体特有必需蛋白,参与早期APR的组装,其缺失会导致子细胞无法形成;2)CGP蛋白参与类锥复合体组装的中后期过程,是维持PCRs结构稳定的关键因子,其缺失会导致成熟虫体缺失PCRs结构,进而导致位于该结构的关键运动相关蛋白(如FRM1)消失,最终使虫体完全丧失运动能力。
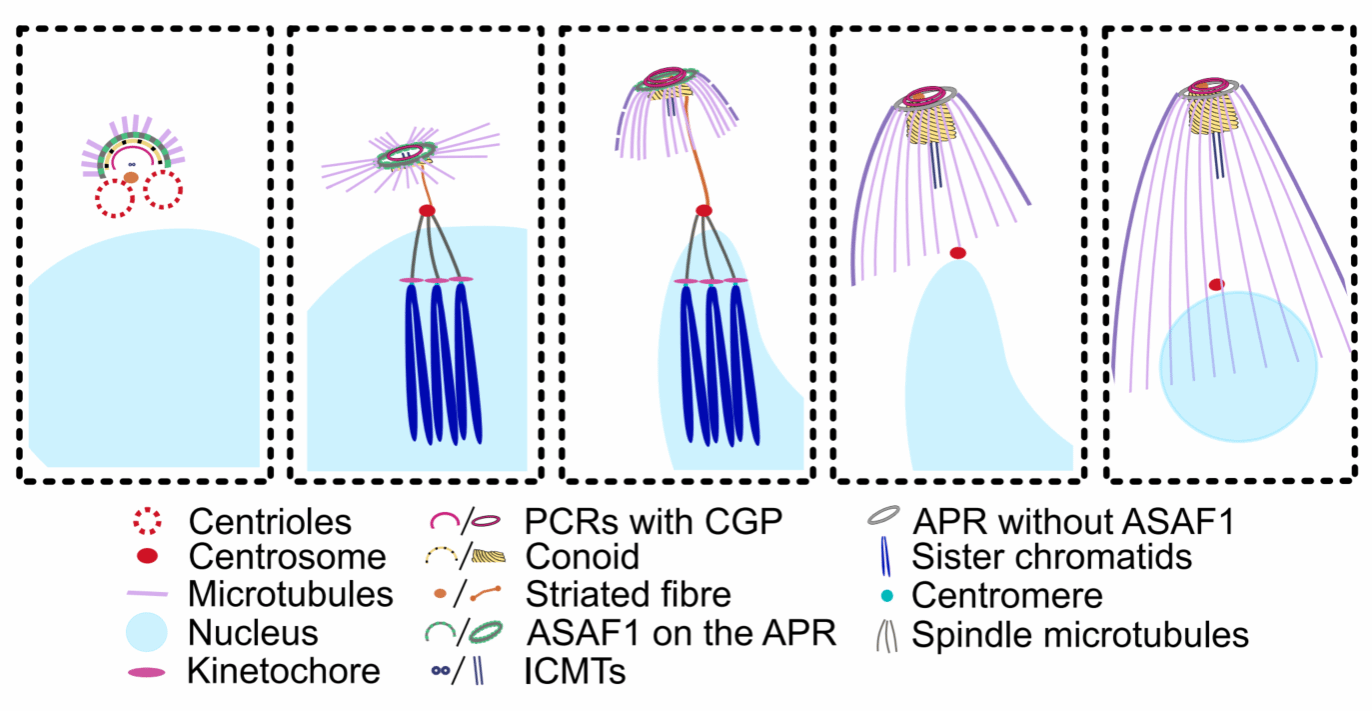
该研究解析了弓形虫类锥复合体组装的分子机制,为深入理解其内二芽殖过程提供了新视角。通过靶向早期组装因子ASAF1,可有效阻断弓形虫在宿主细胞内的增殖,最终虫体死亡,为开发针对寄生虫组装关键环节的新型药物策略奠定了理论基础。
原文链接:https://www.nature.com/articles/s41467-025-65382-y

